Una mirada a la edición genética en México
Ciudad de México. 21 de febrero de 2017 (Agencia Informativa Conacyt).- CRISPR o CRISPR/Cas9 es una herramienta que permite editar el genoma de cualquier célula. Funciona como una tijera molecular, que al entrar al núcleo de las células localiza una región específica y corta la hebra de ácido desoxirribonucleico (ADN), que después será reparada gracias a los mecanismos naturales de las células. Esto da a los científicos la capacidad de inactivar, modificar o añadir genes a las células.
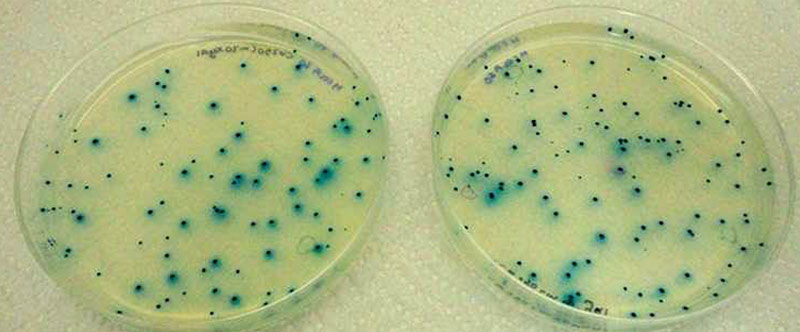
Esta tecnología revolucionaria ha estado nominada dos veces al Premio Nobel, aunque no se le ha otorgado el reconocimiento, la comunidad científica prevé que será reconocida con este galardón tarde o temprano.
Este sistema se empezó a describir como un sistema de defensa que usan las bacterias y las arqueas contra elementos genéticos foráneos, principalmente contra bacteriófagos, estos virus capaces de infectar bacterias que son los mayores depredadores de los microorganismos.
Este tipo de inmunidad en las bacterias les permite cortar pequeños fragmentos del ADN de un virus, o de cualquier ácido nucleico libre, para introducirlo a su propio material genético y así, durante la siguiente infección, responder más eficientemente al ataque del bacteriófago.
Estas capacidades de cortar y pegar ADN externo al genoma propio son las que aprovecha el sistema de edición genética CRISPR/Cas9, para editar en el laboratorio el genoma de células animales y vegetales.
CRISPR no es la técnica de edición más nueva, pero sí es mucho más sencilla, bastante específica e incluso permite editar más de un sitio del genoma, comenta Jorge Meléndez Zajgla, jefe del Laboratorio de Genómica Funcional del Cáncer, del Instituto Nacional de Medicina Genómica (Inmegen).
En México, la Universidad Nacional Autónoma de México (UNAM), el Centro de Investigación y de Estudios Avanzados (Cinvestav) del Instituto Politécnico Nacional (IPN) y el Inmegen realizan investigaciones donde CRISPR/Cas9 es utilizado como apoyo en la investigación básica para mejorar la calidad de plantas de interés alimenticio y para desarrollar una nueva medicina genómica, respectivamente.
¿Qué es CRISPR?
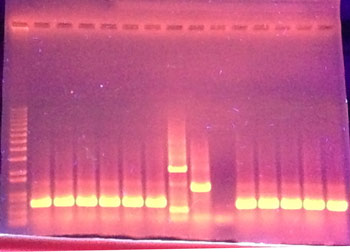 Foto de Liliana Medina.A principios de los años 90, científicos en Japón y España encontraron una región del ADN que contenía una gran cantidad de secuencias palindrómicas cortas, es decir, que se podían leer de igual forma al derecho y al revés. Estas secuencias estaban espaciadas regularmente por pequeños fragmentos de ADN, parecido a las cuentas en un collar.
Foto de Liliana Medina.A principios de los años 90, científicos en Japón y España encontraron una región del ADN que contenía una gran cantidad de secuencias palindrómicas cortas, es decir, que se podían leer de igual forma al derecho y al revés. Estas secuencias estaban espaciadas regularmente por pequeños fragmentos de ADN, parecido a las cuentas en un collar.
Al proseguir con los estudios sobre esta región del genoma bacteriano, los científicos descubrieron que las secuencias de ADN que separaban los segmentos palindrómicos eran muy parecidas al ADN proveniente de virus y de plásmidos, que son secuencias de material genético que circula libre.
En 2002, el científico español Francisco Mojica le dio a esta región de ADN el nombre de CRISPR y, en el año 2005, propuso que CRISPR era un mecanismo de defensa que las bacterias utilizaban para combatir las infecciones por virus o la invasión por ADN extraño.
Esto fue comprobado en el 2007, cuando un grupo de investigadores de la industria alimentaria, quienes demostraron con cepas productoras de yogur que, después de haber sido infectadas por un bacteriófago, las bacterias añadían secuencias espaciadoras a la región CRISPR de su genoma.
Bacterias con memoria inmunológica
“Lo novedoso de CRISPR es que es un sistema de defensa que crea una memoria. Hasta ahora, es el único sistema de defensa que conocemos que permite a las bacterias tener una inmunidad adaptativa y que tiene especificidad. Cuando un virus o un plásmido entra a una bacteria, la bacteria añade una secuencia del genoma del virus o del plásmido como espaciador dentro de la secuencia CRISPR, y son estos pedacitos de ADN los que le permiten identificar y combatir al plásmido o virus específico en una siguiente infección”, explica Liliana Medina Aparicio, estudiante de doctorado en ciencias bioquímicas de la UNAM, quien trabaja analizando el sistema CRISPR en Salmonella Typhi.
Después del descubrimiento publicado en 2007, se empezaron a caracterizar todos los elementos que formaban el sistema CRISPR y se descubrió un grupo de proteínas que ayudaban a que este sistema de defensa funcionara, a estas proteínas se les llamó Cas, en inglés (sistema asociado a CRISPR).
Dentro del variado grupo de proteínas Cas, las más interesantes son las encargadas de cortar el ADN viral y las encargadas de integrar estos pedazos de ADN en un sitio específico del genoma de la bacteria, ese sitio específico es CRISPR, explica la estudiante de doctorado.
Y es justamente esta capacidad del sistema CRISPR/Cas de integrar un ADN externo en un sitio muy específico del ADN, la que fue utilizada para desarrollar una técnica de edición genética.
La tijera genética
La edición genómica en los laboratorios fue posible gracias al trabajo de las científicas Jennifer Doudna y Emmanuelle Charpentier, quienes descubrieron que mediante la proteína Cas9 era mucho más simple que otras y podía cortar en un sitio específico de ADN.
 Thonatiuh con la tijera genética.Además, las investigadoras descubrieron un método para dirigir a Cas9 hacia cualquier sitio del genoma y realizar un corte en cualquier sitio diferente del sitio CRISPR. A partir de ese momento, CRISPR/Cas9 ha sido utilizada para modificar el genoma de diferentes organismos animales y vegetales.
Thonatiuh con la tijera genética.Además, las investigadoras descubrieron un método para dirigir a Cas9 hacia cualquier sitio del genoma y realizar un corte en cualquier sitio diferente del sitio CRISPR. A partir de ese momento, CRISPR/Cas9 ha sido utilizada para modificar el genoma de diferentes organismos animales y vegetales.
¿Cómo se usa la tijera genética en México?
CRISPR es una herramienta con una gran cantidad de aplicaciones. Lo más sencillo es utilizar la enzima para que corte una región específica del genoma, corte que será reparado por las células, pero generalmente de una manera imprecisa que termina por inactivar el gen. Otras de sus funciones, y tal vez las más conocidas, son la reparación de daños y la introducción de nuevos genes en el genoma, pero estos son métodos más complicados, explica Jorge Meléndez.
En México, instituciones como la UNAM, el Cinvestav y el Inmegen comienzan a utilizar esta herramienta de edición genética con miras a generar nuevos métodos de medicina genómica, a mejorar la calidad de los cultivos agrícolas y a volver más sostenible esta industria, y como herramienta esencial en la ciencia básica.
CRISPR para mejorar el cultivo de alimentos
En el Laboratorio Nacional de Genómica para la Biodiversidad (Langebio) del Cinvestav, desde hace un año se encuentran trabajando con la técnica CRISPR con el objetivo de incorporar características benéficas a especies de plantas comerciales como el maíz, la soya y el arroz. Estas modificaciones podrían ayudar a los cultivos a resistir las inclemencias del tiempo, o incluso disminuir la cantidad de agroquímicos que requieren para crecer.
Estas características pueden ser incorporadas al integrar en la planta variedades de genes que se encuentran dentro de su misma especie. Estas variedades se denominan alelos, y son formas alternativas de un gen que se encuentran naturalmente presentes dentro de la diversidad biológica de la especie.
Por ejemplo, existe un solo gen que controla la herencia del grupo sanguíneo ABO, pero este gen tiene tres alelos, tres variantes, la que confiere el tipo de sangre A, la que confiere el tipo de sangre B y la que confiere el tipo de sangre O.
En las plantas, estas variedades de genes pueden otorgarles resistencia a ciertas condiciones ambientales o la capacidad de producir una mayor cantidad de cierto compuesto.
Por esta razón, el equipo de investigación del Langebio, liderado por el doctor Luis Herrera Estrella, trabaja para incorporar alelos presentes en variedades no comerciales de las pantas a la variedad comercial de la planta.
Este intercambio de alelos se viene realizando, mediante cruzas, desde hace miles de años, a lo que llamamos programas de mejoramiento genético tradicional, explica el investigador.
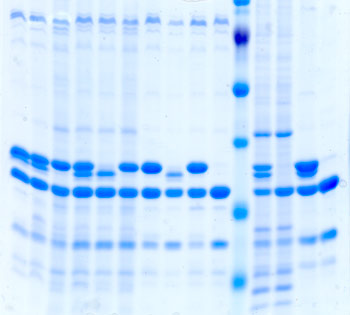 Gel de proteínas.Los métodos tradicionales toman una variedad comercial y la cruzan con la variedad silvestre que tiene la versión del gen que se desea. La planta obtenida no tiene todas las características de su progenitor comercial, por lo que debe retrocruzarse entre seis o siete veces para regresarle las características deseadas presentes en la variedad comercial, pero conservando el nuevo alelo de la especie silvestre.
Gel de proteínas.Los métodos tradicionales toman una variedad comercial y la cruzan con la variedad silvestre que tiene la versión del gen que se desea. La planta obtenida no tiene todas las características de su progenitor comercial, por lo que debe retrocruzarse entre seis o siete veces para regresarle las características deseadas presentes en la variedad comercial, pero conservando el nuevo alelo de la especie silvestre.
“Este es un proceso bastante largo, pero si utilizamos CRISPR podemos modificar el gen que nos interesa directamente en la variedad comercial y mantener el resto de su genoma intacto”, detalla Luis Herrera, director del Langebio.
Incluso, existe la posibilidad de introducir diferentes alelos en un solo proceso. Algo que llevaría una gran cantidad de cruzas podría realizarse de una manera mucho más rápida gracias a la edición genómica, comenta el investigador.
Plantas resistentes a la sequía
Luis Herrera explica que CRISPR también ofrece la posibilidad de modificar la expresión del genoma, es decir, ayudar a que un gen que ya se encuentra en una planta se active o desactive en respuesta a elementos del ambiente.
“Por ejemplo, nosotros estudiamos una propiedad muy interesante que tienen las semillas que sobreviven secas durante mucho tiempo. Estas semillas contienen un embrión que se puede almacenar incluso por décadas y que sigue teniendo la capacidad de producir una planta. Este asombroso sistema, para protegerse contra la desecación, queremos llevarlo a las hojas para que logren tolerar la sequía”, detalla el director del Langebio.
Esto requiere modificar la planta de tal manera que esos mismos genes que activa, en su estado de semilla, los logre activar siendo adulta cuando se encuentra en condiciones de sequía. Posibilidad real con el sistema CRISPR/Cas.
CRISPR para combatir la fiebre tifoidea
El sistema CRISPR se encuentra en 90 por ciento de los genomas de las arqueas y 45 por ciento de los genomas de las bacterias que se han secuenciado. Sin embargo, no todos los microorganismos utilizan CRISPR como un sistema de defensa. Hay algunos indicios que apuntan a que CRISPR está involucrado en procesos fisiológicos, como la formación de esporas, que le confieren virulencia a las bacterias, comenta Liliana Medina.
Este es el caso de Salmonella Typhi, bacteria causante de la fiebre tifoidea, en la cual CRISPR parece estar involucrada en la habilidad del microorganismo para causar enfermedades graves en el humano.
Por ello, en el Instituto de Biotecnología de la UNAM, el doctor Ismael Hernández Lucas dirige la tesis de doctorado de Liliana Medina que busca dilucidar el papel que tiene CRISPR en la virulencia de esta bacteria, causante de la fiebre tifoidea.
“Aún no se conocen todos los mecanismos de virulencia de este patógeno, por eso queremos saber si CRISPR tiene algo que ver con la capacidad infecciosa de Salmonella. Este trabajo de ciencia básica nos dará herramientas para entender cómo funciona la bacteria y así saber cómo atacarla. Incluso podríamos modificar el sistema CRISPR para que la bacteria por sí sola active o desactive algún gen que la haga inofensiva para el ser humano”, explica Liliana Medina.
CRISPR para estudiar el “nuevo genoma”
 Larvas silvestres con knock out.En el Inmegen, se utiliza la técnica CRISPR desde hace casi tres años, cuando el doctor Jorge Meléndez intentó replicar la técnica desde el artículo original.
Larvas silvestres con knock out.En el Inmegen, se utiliza la técnica CRISPR desde hace casi tres años, cuando el doctor Jorge Meléndez intentó replicar la técnica desde el artículo original.
Jorge Meléndez comenzó utilizando CRISPR para cortar e inactivar genes que producen ácidos ribonucleicos (ARN) largos no codificantes, que son un tipo de ARN que no se traduce en una proteína pero que ayuda a regular diferentes procesos celulares, incluyendo la producción de otras proteínas.
Estos ARN son muy interesantes, explica Jorge Meléndez, pues hasta hace poco se pensaba que una gran cantidad del genoma era material que no se utilizaba, incluso en algún momento se le llamó ADN basura. Pero se descubrió que eso no es verdad, y que la mayoría del ADN que se transcribe sí tiene una función. De estos transcritos que sí tienen función, la mayoría son ARN largos no codificantes.
“El ser humano tiene entre 21 y 23 mil genes que codifican a proteínas, pero de ARN largo no codificante suponemos que va a haber alrededor de 60 mil. Estos son genes que no sabemos qué hacen, y para estudiar su función lo que estamos haciendo con células troncales, en modelos de cáncer, es utilizar CRISPR para averiguar su función. Si de alguna manera podemos suprimir la actividad del gen, entonces podremos estudiar su función”, detalla el investigador.
Al inactivar estos genes, el equipo de investigación de Jorge Meléndez puede estudiar la función de los ARN largos no codificantes, principalmente su papel en el desarrollo del cáncer.
Edición del genoma para estudiar el cáncer
Además de estudiar los ARN largos no codificantes, cuyas características podrían aprovecharse para tratamientos contra el cáncer, por ejemplo, bloqueando la producción de proteínas que las células cancerígenas necesitan para crecer, el grupo de investigación utiliza CRISPR para inactivar o modificar diferentes genes supresores de tumor y oncogenes y conocer su función en el desarrollo del cáncer.
Estos análisis se hacen en cultivos celulares de células cancerígenas, o en peces cebra, y se trabaja con cáncer de pulmón, de páncreas, cervicouterino, tumores infantiles. “Cuando encontramos un gen con características interesantes es cuando decidimos investigarlo a fondo con CRISPR”, explica Jorge Meléndez.
Mejorando CRISPR
A pesar de que CRISPR es una herramienta que supera en eficiencia y costo las técnicas de edición genética que se utilizaban hasta el momento, aún tiene una limitante que dificulta su aplicación en el campo de la medicina humana: solo pueden modificarse, eficientemente, células que se reproducen constantemente, por ejemplo las embrionarias, dejando fuera las neuronas y otro tipo de células, como las del ojo, que se dividen muy ocasionalmente.
Para resolver este problema, un grupo de científicos que trabaja en el Instituto Salk de Estados Unidos ideó una técnica que permite emplear el sistema CRISPR/Cas, pero añadiéndole un componente que posibilita modificar el genoma de células maduras de individuos adultos. A esta nueva metodología de edición genética la llamaron HITI.
En esta revolucionaria investigación participa una joven mexicana, Reyna Hernández Benítez, quien explica que CRISPR/Cas introduce una nueva secuencia de ADN a las células, pero necesita de la maquinaria que la célula utiliza normalmente para reproducirse, con el fin de integrar el nuevo material genético. Esto obligaba a los científicos a forzar a células a reproducirse, algo que no era natural.
 Peces cebra mosaico para gen torosinasa.Este problema lo soluciona HITI, pues en vez de utilizar el mecanismo de reproducción de la célula para integrar el nuevo ADN, usa sus mecanismos de reparación, que se encuentran constantemente activos, para corregir errores causadas por la exposición a rayos ultravioleta y todo tipo de mutágenos.
Peces cebra mosaico para gen torosinasa.Este problema lo soluciona HITI, pues en vez de utilizar el mecanismo de reproducción de la célula para integrar el nuevo ADN, usa sus mecanismos de reparación, que se encuentran constantemente activos, para corregir errores causadas por la exposición a rayos ultravioleta y todo tipo de mutágenos.
Recuperando la visión en retinitis pigmentosa
El grupo de investigación, al cual pertenece Reyna Hernández, decidió probar la nueva técnica para corregir una mutación el gen MERTK, que ocasiona ceguera por retinitis pigmentosa.
Los científicos decidieron hacer la experimentación en ratas adultas, con ceguera por mutación en el gen. Les realizaron una inyección en el ojo para introducirles el sistema CRISPR/Cas, que se encargaría de dirigir el nuevo ADN a la región adecuada, además de la molécula HITI, que permitiría integrar la nueva secuencia al genoma y corregir los efectos de la mutación.
“Afortunadamente corroboramos nuestro resultado, se demostró que la respuesta visual de las ratas se mejoraba con el tratamiento… Este es un resultado alentador, pues nos indica que justamente estamos en el inicio de una nueva historia”, comenta la investigadora mexicana.
Las correcciones que realizó HITI en el genoma de las ratas resultaron ser bastante exactas, es decir, las modificaciones no afectaron otras partes del ADN. Pero aún falta mejorar el número de células editadas con esta técnica para mejorar la respuesta a la terapia. Pues las células tienen muchos mecanismos que impiden la entrada de material genético extraño a su interior y evitan que HITI logre corregir el genoma, explica Reyna Hernández.
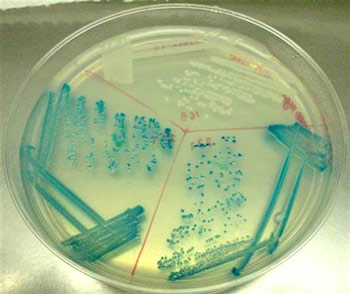 Placa.La investigadora considera que el perfeccionamiento de esta técnica permitiría desarrollar tratamientos para problemas en código genético de células del ojo, corazón, cerebro o páncreas, incluso en individuos adultos que ya presentan una enfermedad.
Placa.La investigadora considera que el perfeccionamiento de esta técnica permitiría desarrollar tratamientos para problemas en código genético de células del ojo, corazón, cerebro o páncreas, incluso en individuos adultos que ya presentan una enfermedad.
Cambiando el mundo de la edición genética
Luis Herrera, director del Langebio, considera que CRISPR/Cas tiene un potencial extraordinario, pues permitirá realizar modificaciones genéticas de una forma más rápida, precisa y versátil. Sobre todo permitirá insertar, eliminar o modificar genes en el lugar exacto donde se desea realizar la modificación, y evitará modificaciones en otras partes del genoma, que podrían tener efectos secundarios.
CRISPR se presenta como una herramienta revolucionaria pero que aún requiere de mucho desarrollo tecnológico para estar completa. Por el momento es fácil desactivar genes, introducir aminoácidos en una nueva proteína es un poco más complicado, pero reemplazar un gen por otro es algo que se ha logrado pero que es técnicamente más difícil. Sin embargo, seguramente en los próximos dos o tres años veremos estas técnicas aplicadas con mayor efectividad y eficiencia, considera el investigador.
Para Jorge Meléndez, del Inmegen, existe la esperanza de que aproximadamente en cinco años esta herramienta permita sacar células dañadas del cuerpo, modificarlas y regresarlas para tratar enfermedades genéticas raras en niños, enfermedades hepáticas y un sinfín de afecciones humanas.

Esta obra cuyo autor es Agencia Informativa Conacyt está bajo una licencia de Reconocimiento 4.0 Internacional de Creative Commons.

